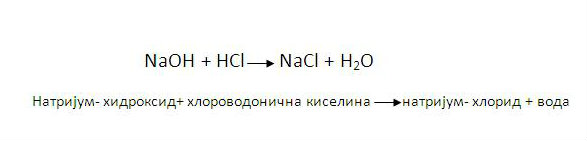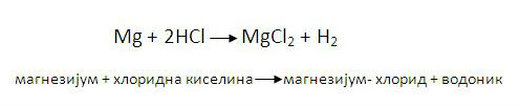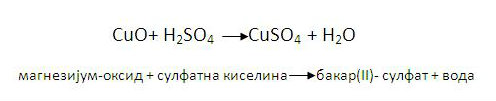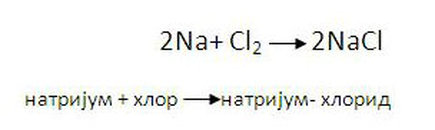Соли
-Соли су јонска једињења која садрже позитивне јоне метала и негативне јоне киселинског остатка.
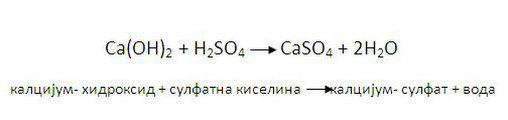
-У реакцији базе са киселином настају со и вода.
-Реакција у којој настају со и вода назива се неутрализација.
-У реакцији базе са киселином настају со и вода.
-Реакција у којој настају со и вода назива се неутрализација.
Именовање соли
-Соли добијају назив према називу метала и јона киселинског остатка.
Добијање соли
-Соли добијају назив према називу метала и јона киселинског остатка.
Добијање соли
- реакција неутрализације
2. реакција метала и киселина
-Већина метала реагује са киселина и при тој реакцији отпушта водоник
метал + киселина → со + водоник
-Већина метала реагује са киселина и при тој реакцији отпушта водоник
метал + киселина → со + водоник
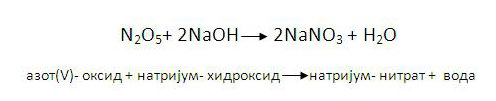
3. реакција киселих оксида и база
-Кисели оксиди са водом граде киселине.
-У реакцији са базама кисели оксиди дају соли.
кисели оксид + база →со + вода
-Кисели оксиди са водом граде киселине.
-У реакцији са базама кисели оксиди дају соли.
кисели оксид + база →со + вода
4. реакција базних оксида и киселина
-Базни оксиди са киселинама граде соли
базни оксид + киселина→со + вода
-Базни оксиди са киселинама граде соли
базни оксид + киселина→со + вода
5. директна синтеза из елемената
-Соли се могу добити синтезом два елемента
метал + неметал→со
-Соли се могу добити синтезом два елемента
метал + неметал→со
Физичка својства соли
-Соли су у чврстом агрегатном стању.
-Алкални и земноалкални метали граде соли беле боје, а прелазни метали граде обојене соли.
-Према растворљивости могу се делити на добро растворљиве и славо растворљиве.
-Соли које се добро растварају су: натријум- хлорид, натријум- нитрат, натријум- карбонат...
-Соли које се слабо растварају су: калцијум- карбонат, баријум-сулфат, сребро- хлорид...
Хемијска реакција соли
-Соли су слабо реактивна једињења.
-Реагују са киселинама, базама и солима ако се при реакцији ослобађа гас или ствара талог.
*реакција замене је реакција у којима долази до замене атома или атомских група.
ВАЖНЕ СОЛИ
-Кухињска со(NaCl)
Натријум- хлорид познатији као кухињска со користи се као зачин јелима, а користи се и у медицини.
-Сода бикарбона(NaHCO3)
Сода бикарбона користи се као "пекарски" прашак.
-Сода(Na2CO3)
Соду у природи можемо наћи на местима где је некада било језеро. Најзначајнију примену има у индустрији стакла и средстава за прање.
-Плави камен(CuSO4)
Плави камен (бакар(II)- сулфат пентахидрат) употребљава се у пољопривреди за заштиту винове лозе.
-Гипс(CaSO4 * 2H2O)
Гипс се користи у грађавинарству и у медицини
-Соли су у чврстом агрегатном стању.
-Алкални и земноалкални метали граде соли беле боје, а прелазни метали граде обојене соли.
-Према растворљивости могу се делити на добро растворљиве и славо растворљиве.
-Соли које се добро растварају су: натријум- хлорид, натријум- нитрат, натријум- карбонат...
-Соли које се слабо растварају су: калцијум- карбонат, баријум-сулфат, сребро- хлорид...
Хемијска реакција соли
-Соли су слабо реактивна једињења.
-Реагују са киселинама, базама и солима ако се при реакцији ослобађа гас или ствара талог.
*реакција замене је реакција у којима долази до замене атома или атомских група.
ВАЖНЕ СОЛИ
-Кухињска со(NaCl)
Натријум- хлорид познатији као кухињска со користи се као зачин јелима, а користи се и у медицини.
-Сода бикарбона(NaHCO3)
Сода бикарбона користи се као "пекарски" прашак.
-Сода(Na2CO3)
Соду у природи можемо наћи на местима где је некада било језеро. Најзначајнију примену има у индустрији стакла и средстава за прање.
-Плави камен(CuSO4)
Плави камен (бакар(II)- сулфат пентахидрат) употребљава се у пољопривреди за заштиту винове лозе.
-Гипс(CaSO4 * 2H2O)
Гипс се користи у грађавинарству и у медицини