Поновимо...
Крај 19. и почетак 20. века - атом сложена честица
Шта су атоми?
Атоми су честице лоптастог облика, веома малих димензија и масе
Шта су атоми?
Атоми су честице лоптастог облика, веома малих димензија и масе
Грађа атома
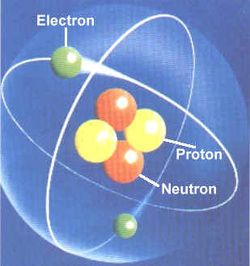
У језгру атома налазе се нуклеони(протони и неутрони)
У електронском омотачу се налазе електроне.
-Атом садржи исти број протона и неутрона. Тј. за сваки атом важи: N(p+) = N(e-)
-Количина позитивног наелектрисања, једнака је количини негативног наелектрисања g+=g-
Што значи:
Атом је у целини ненаелектрисана честица(електронеутрална или неутрална честица).
Једине покретне честице су електроне.
m(p+) приближно је једнака m(n°)
m(p+) > m(e-) (маса протона је од масе електрона већа 2000 пута)
Атоми свих елемената имају језгро и електронски омотач. А атоми различитих елемената се разликују по броју протона.
Атомски број Z
Масени број A
Атомски број означава протона у језгру.
Масени број означава збир протона и неутрона.
Z<A (атомски број је увек мањи од масеног броја)
Изотопи су атоми истог елемента који имају исти број протона у језгру, а различит број неутрона. Значи, изотопи се разликују по масеном броју.
-протиум ( један протон, што значи да су и атомски и масени број исти)
-деутеријум ( један протон и један неутрон, атомски број је један, масени број је два) - АТОМ ВОДОНИКА
-трицијум ( један протон и два неутрона, атомски број један, масени број три)
У електронском омотачу се налазе електроне.
- Протони (p+) су носиоци позитивног наелектрисања, садрже јединицу позитивног наелектрисања.
- Неутрони (n°) су неутралне или ненаелектрисане честице.
- Електроне (e-) су негативно наелектрисане честице, носиоци јединице негативног наелектрисања.
-Атом садржи исти број протона и неутрона. Тј. за сваки атом важи: N(p+) = N(e-)
-Количина позитивног наелектрисања, једнака је количини негативног наелектрисања g+=g-
Што значи:
Атом је у целини ненаелектрисана честица(електронеутрална или неутрална честица).
Једине покретне честице су електроне.
m(p+) приближно је једнака m(n°)
m(p+) > m(e-) (маса протона је од масе електрона већа 2000 пута)
Атоми свих елемената имају језгро и електронски омотач. А атоми различитих елемената се разликују по броју протона.
Атомски број Z
Масени број A
Атомски број означава протона у језгру.
Масени број означава збир протона и неутрона.
Z<A (атомски број је увек мањи од масеног броја)
Изотопи су атоми истог елемента који имају исти број протона у језгру, а различит број неутрона. Значи, изотопи се разликују по масеном броју.
-протиум ( један протон, што значи да су и атомски и масени број исти)
-деутеријум ( један протон и један неутрон, атомски број је један, масени број је два) - АТОМ ВОДОНИКА
-трицијум ( један протон и два неутрона, атомски број један, масени број три)
